ALCANOS:
El primer miembro de la familia de los alcanos es el metano. Está formado por un átomo de carbono, rodeados de 4 átomos de hidrógeno.
Fórmula desarrollada:
Fórmula molecular: CH4

Los demás miembros se diferencian en el agregado de un átomo de carbono. Los nombres de los más conocidos son:
Etano: dos átomos de C.
Propano: Tres átomos de C.
Butano: Cuatro átomos de C.
Pentano: Cinco átomos de C.
Hexano: Seis átomos de C.
Heptano: Siete átomos de C.
Octano: Ocho átomos de C.
Nonano: Nueve átomos de C.
Decano: Diez átomos de C.
Algunas fórmulas:
Etano:
H3C —- CH3
Propano:
H3C —- CH2 —- CH3
Pentano:
H3C —- CH2 —– CH2 —– CH2 —– CH3
Para concluir decimos que los alcanos presentan la siguiente fórmula molecular (CnH2n+2). Donde n es la cantidad de átomos de Carbono y (2n+2) nos da la cantidad de átomos de hidrógeno.
Propiedades físicas:
Los alcanos son parte de una serie llamada homóloga. Ya que cada término se diferencia del que le continúa en un CH2. Esto nos ayuda a entender sus propiedades físicas ya que sabiendo la de algunas podemos extrapolar los resultados a las demás. Las principales características físicas son:
Los cuatro primeros miembros bajo condiciones normales o en su estado natural son gaseosos.
Entre el de 5 carbonos y el de 15 tenemos líquidos y los restantes sólidos.
El punto de ebullición asciende a medida que crece el número de carbonos.
Todos son de menor densidad que el agua.
Son insolubles en el agua pero solubles en solventes orgánicos.
Propiedades Químicas:
Presentan muy poca reactividad con la mayoría de los reactivos químicos. Por este motivo se los llama también parafinas.
El ácido sulfúrico, hidróxido de sodio, ácido nítrico y ciertos oxidantes los atacan solo a elevada temperatura.
CH3 — CH3 —————-> CH3 — CH2 NO2 + H2O (a 430°C y en presencia de HNO3)
Combustión:
CH3 — CH3 + 7/2 O2 ——> 2 CO2 + 3 H2O + 372,8 Kcal
Compuestos de Sustitución:
Las reacciones de sustitución son aquellas en las que en un compuesto son reemplazados uno o más átomos por otros de otro reactivo determinado.
Loa alcanos con los halógenos reaccionan lentamente en la oscuridad, pero más velozmente con la luz.
CH4 + Cl2 —–> CH3Cl + HCl
metano (luz) cloruro de metilo
ALQUENOS:
Los alquenos se diferencian con los alcanos en que presentan una doble ligadura a lo largo de la molécula. Esta condición los coloca dentro de los llamados hidrocarburos insaturados junto con los alquinos. Con respecto a su nomenclatura es como la de los alcanos salvo la terminación. En lugar de ano como los alcanos es eno. Al tener una doble ligadura hay dos átomos menos de hidrógeno como veremos en las siguientes estructuras. Por lo tanto, la fórmula general es CnH2n.
Explicaremos a continuación como se forma la doble ligadura entre carbonos.
Anteriormente explicamos la hibridación SP3. Esta vez se produce la hibridación Sp2. El orbital 2s se combina con 2 orbitales p, formando en total 3 orbitales híbridos llamados Sp2. El restante orbital p queda sin combinar. Los 3 orbitales Sp2 se ubican en el mismo plano con un ángulo de 120° de distancia entre ellos.

El orbital p que no participo en la hibridación ocupa un lugar perpendicular al plano que sostiene a los tres orbitales Sp2.
El enlace doble se forma de la siguiente manera:
Uno de los orbitales sp2 de un C se enlaza con otro orbital sp2 del otro C formando un enlace llamado sigma. El otro enlace está constituido por la superposición de los enlaces p que no participaron en la hibridación. Esta unión se denomina Pi (∏).
Así tenemos por ejemplo Eteno, Propeno, Buteno, etc.
Al nombrar Alquenos y Alquinos a la doble o triple ligadura se le adjudica un número que corresponde a la ubicación de dicha ligadura.
Eteno:
CH2 = CH2
Propeno:
CH2 = CH2 –CH3
Buteno – 1
CH2 = CH — CH2 — CH3
Buteno – 2
CH3 – CH = CH — CH3
Pentino – 2
CH3 — C ≡ C — CH2 —-CH3
Propiedades Físicas:
Son similares a los alcanos. Los tres primeros miembros son gases, del carbono 4 al carbono 18 líquidos y los demás son sólidos.
Son solubles en solventes orgánicos como el alcohol y el éter. Son levemente más densos que los alcanos correspondientes de igual número de carbonos. Los puntos de fusión y ebullición son más bajos que los alcanos correspondientes. Es interesante mencionar que la distancia entre los átomos de carbonos vecinos en la doble ligadura es más pequeña que entre carbonos vecinos en alcanos. Aquí es de unos 1.34 amstrong y en los alcanos es de 1.50 amstrong.
Propiedades Químicas:
Los alquenos son mucho más reactivos que los Alcanos. Esto se debe a la presencia de la doble ligadura que permite las reacciones de adición. Las reacciones de adición son las que se presentan cuando se rompe la doble ligadura, este evento permite que se adicionen átomos de otras sustancias.
Adición de Hidrógeno:→
En presencia de catalizadores metálicos como níquel, los alquenos reaccionan con el hidrógeno, y originan alcanos.
CH2 = CH2 + H2 ——> CH3 – CH3 + 31,6 Kcal
Adición de Halógenos
CH2 = CH2 + Br2 ——-> CH2Br – CH2Br
Dibromo 1-2 Etano
Adición de Hidrácidos:
CH2 = CH2 + HBr ——-> CH3 — CH2 Br
Monobromo Etano
Cuando estamos en presencia de un alqueno de más de 3 átomos de carbono se aplica la regla de Markownicov para predecir cuál de los dos isómeros tendrá presencia mayoritaria.
H2C = CH — CH3 + H Cl → H3C — CHBr — CH3 monobromo 2 – propano
→ H3C — CH2 — CH2Br monobromo 1 – propano
Al adicionarse el hidrácido sobre el alqueno, se formara casi totalmente el isómero que resulta de unirse el halógeno al carbono más deficiente en hidrógeno. En este caso se formara más cantidad de monobromo 2 – propano.
Combustión:
Los alquenos también presentan la reacción de combustión, oxidándose con suficiente oxigeno.
C2H4 + 3 O2 —-> 2 CO2 + 2 H2O
Etano
Diolefinas:
Algunos Alquenos poseen en su estructura dos enlaces dobles en lugar de uno. Estos compuestos reciben el nombre de Diolefinas o Dienos. Se nombran como los Alcanos, pero cambiando le terminación ano por dieno.
H2C = C = CH2
Propadieno – 1,3
H2C = CH — CH = CH2
Butdieno – 1,3
ALQUINOS:
Estos presentan una triple ligadura entre dos carbonos vecinos. Con respecto a la nomenclatura la terminación ano o eno se cambia por ino. Aquí hay dos hidrógenos menos que en los alquenos. Su fórmula general es CnH2n-2. La distancia entre carbonos vecinos con triple ligadura es de unos 1.20 amstrong.
Para la formación de un enlace triple, debemos considerar el otro tipo de hibridación que sufre elátomo de C. La hibridación “sp”.
En esta hibridación, el orbital 2s se hibridiza con un orbital p para formar dos nuevos orbitales híbridos llamados “sp”. Por otra parte quedaran 2 orbitales p sin cambios por cada átomo de C.
El triple enlace que se genera en los alquinos está conformado por dos tipos de uniones. Por un lado dos orbitales sp solapados constituyendo una unión sigma. Y las otras dos se forman por la superposición de los dos orbitales p de cada C. (Dos uniones ∏).
Ejemplos:
Propino
CH ≡ C — CH3
Propiedades físicas:
Los dos primeros son gaseosos, del tercero al decimocuarto son líquidos y son sólidos desde el 15 en adelante.
Su punto de ebullición también aumenta con la cantidad de carbonos.
Los alquinos son solubles en solventes orgánicos como el éter y alcohol. Son insolubles en agua, salvo el etino que presenta un poco de solubilidad.
Propiedades Químicas:
Combustión:
2 HC ≡ CH + 5 O2 ——> 4 CO2 + 2 H2O + 332,9 Kcal
Adición de Halógenos:
HC ≡ CH —- CH3 + CL2 —> HCCl = CCl — CH3
Propino ,2 – dicloro propeno
Adición de Hidrógeno: Se usan catalizadores metálicos como el Platino para favorecer la reacción.
HC ≡ C —- CH3 + H2 ——> H2C = CH — CH3
Propino Propeno
Se puede continuar con la hidrogenación hasta convertirlo en alcano si se lo desea.
Adición de Hidrácidos:
HC ≡ CH —- CH3 + HBr —-> H2C = C Br —- CH3
Propino – 1 Bromo – 2 – Propeno
Como se observa se sigue la regla de Markownicov. Ya que el halógeno se une al carbono con menos hidrógenos. En este caso al del medio que no tiene ninguno.
Ahora vamos a explicar como se denominan a los hidrocarburos con ramificaciones.
 Aquí podemos ver que tenemos dos ramificaciones. Los grupos que forman esa ramificación son considerados radicales. Radical en química es un átomo o grupo de átomos que posee una valencia libre. Esta condición los hace susceptibles a unirse a cadenas carbonadas en este caso.
Aquí podemos ver que tenemos dos ramificaciones. Los grupos que forman esa ramificación son considerados radicales. Radical en química es un átomo o grupo de átomos que posee una valencia libre. Esta condición los hace susceptibles a unirse a cadenas carbonadas en este caso.
Obtenemos un radical cuando al metano (CH4) le quitamos un átomo de hidrógeno en su molécula quedándole al carbono una valencia libre.
CH3
Este radical se llama metil o metilo. Su nombre deriva del metano. Se les agrega el sufijo il.
Si lo obtuviéramos a partir del Etano se llamaría etil y a partir del propano, propil y así sucesivamente.
Etil y Propil:
H3C — CH2 –
H3C — CH — CH2 –
A veces se presentan otros radicales cuando el hidrógeno faltante es de un carbono secundario, es decir, que está unido a otros dos carbonos. Si al propano le quitamos un H del C del medio tenemos al radical isopropil:
H3C — CH — CH3
Otros radicales que podemos citar son el isobutil y el ter-butil derivado del butano.
Isopropil e Isobutil

Ter-butil

Volviendo al primer ejemplo de hidrocarburo ramificado.

Vemos claramente una cadena horizontal integrada por 4 átomos de C, y un grupo metilo en la parte superior. Este metil es la ramificación. Se nombra primero a este metil con un número que indica la posición de este en la cadena más larga. El numero uno se le asigna al carbono que está más cerca de la ramificación. Luego nombramos a la cadena.
El nombre es 2 metil-Butano.
Otros ejemplos:

2,2,4-triimetil pentano (Los metilos están ubicados en los carbonos 2 y 4 respectivamente). Se toma como carbono 1 el primero que esta a la izquierda ya que más cerca de este extremo hay más metilos.

Isomería:
Los compuestos hidrocarbonados al tener fórmulas grandes presentan variación en su disposición atómica. Es decir, con la misma fórmula molecular pueden tener varias fórmulas desarrolladas. Esto es la isomería. Aunque tenemos que decir que hay varios tipos de isomería. Aquí explicaremos por ahora la isomería de cadena, o sea, las distintas formas que pueden tomar las cadenas carbonadas.
Por ejemplo, en el caso del Pentano (C5H12), a este lo podemos presentar como una cadena lineal o como cadenas ramificadas.
Pentano (lineal)
H3C — H2C —H2C — H2C — CH3
2-metil Butano (ramificado)

Para ser considerado una ramificación, el radical debe estar en un C que no sea del extremo, es decir, en un C secundario. Si hubiésemos puesto el metil en el otro C secundario, el nombre no hubiera variado ya que la numeración empezaría del otro extremo.
2,2 –dimetil Propano

Los Alquenos y Alquinos también pueden presentar este tipo de isomería al cambiar la posición de sus grupos ramificados. Pero presentan aparte otro tipo de isomería llamada de posición.
En esta isomería lo que varia es la posición del doble o triple enlace. Por ejemplo:
Buteno-1
CH2 = CH — CH2 — CH3
Buteno-2
CH3 — CH = CH — CH3




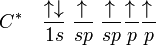

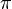 ). Las reglas de ubicación de los electrones en estos casos, como el alqueno etileno obligan a una hibridación distinta llamada sp2, en la cual un electrón del orbital 2s se mezcla sólo con dos de los orbitales 2p: surge a partir o al unirse el orbital s con dos orbitales p; por consiguiente, se producen tres nuevos orbitales sp2, cada orbital nuevo produce enlaces covalentes
). Las reglas de ubicación de los electrones en estos casos, como el alqueno etileno obligan a una hibridación distinta llamada sp2, en la cual un electrón del orbital 2s se mezcla sólo con dos de los orbitales 2p: surge a partir o al unirse el orbital s con dos orbitales p; por consiguiente, se producen tres nuevos orbitales sp2, cada orbital nuevo produce enlaces covalentes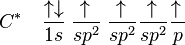
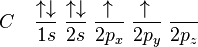

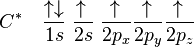
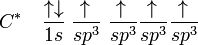


.jpg)
.jpg)
